Relação Criolita-Alumínio

Na natureza, raramente encontramos alumínio puro devido a alta afinidade deste com o oxigênio, sendo que, na maioria das vezes, ele está compondo a estrutura de minerais forma Al3+. Com isso, para obter esse metal é necessário estabelecer métodos para sua extração.
Anteriormente, a produção de alumínio não era viável por ter um custo elevado. Assim, após um período de estudos, foi criado um método que facilita e reduz o custo de extração desse material, denominado Processo de Hall-Héroult. Esse mecanismo retira o alumínio presente na bauxita e, com o auxílio do mineral Criolita, é possível obter Al(s). A partir disso, é interessante compreender a atuação da Criolita no processo de formação do alumínio, conforme iremos explicar ao longo do texto.
O que é a criolita?

A Criolita é um mineral de composição química Na3AlF6, sendo 32,8% Na, 12,8% Al, e 54,4% F. Esse mineral tem como características apresentar brilho vítreo a graxo, cor incolor a branco neve, transparente a translúcido. Ademais, por apresentar baixo índice de refração, a criolita assume características semelhantes as da neve e da parafina, dessa forma, quando pulverizado e imerso em água quase desaparece.
O depósito mais importante de Criolita está localizado em Ivigut na Groenlândia. Entretanto, ela é encontrada também em Miask (Rússia), Colorado (Estados Unidos) e Quebec (Canadá).
Esse mineral era utilizado como fonte de alumínio até ser substituído pela bauxita. Posteriormente, passou a ser empregado no processo de extração do Al na bauxita (Processo de Hall-Héroult). Além disso, é utilizado na produção de alguns vidros e porcelanas e, também, como um produto de limpeza para superfícies metálicas.
Metalurgia do alumínio
Com o intuito de destacar a importância da Criolita no processo de produção do alumínio, é importante considerar duas coisas. Quais eram os principais problemas encontrados para a obtenção do mineral antes do início da utilização da criolita e quais alternativas foram propostas para solucioná-las?
Problemas
Antes de criar alternativas para a extração de alumínio, alguns empecilhos elevavam o custo do processo, restringindo a utilização desse metal. Entre eles destaca-se, principalmente, o elevado ponto de fusão da alumina (Al2O3). Esse óxido de alumínio, presente na bauxita, tem ponto de fusão que atinge, aproximadamente, 2000°C. Devido a essa característica, a alumina faz com que o valor de produção de alumínio seja elevado.
Processo Hall-Héroult
Diante desse problema, Charles M. Hall e Paul Héroult em 1886 desenvolveram um método para produção de alumínio que ficou conhecido como processo Hall-Héuroult. Como matéria prima, foi utilizada a bauxita e dela houve extração da alumina.
Esse material apresenta elevada temperatura de fusão, como visto anteriormente, e a solução para esse problema foi a descoberta, pelos cientistas, do potencial da criolita (Na3AlF6). Ela atua como fundente da alumina reduzindo seu ponto de fusão para cerca de 1000°C.
Assim, com o intuito de reduzir a temperatura de fusão da alumina, uma mistura mistura fundida de (Al2O3+ Na3AlF6), é colocada em um recipiente de ferro ou cobre, provocando a seguinte reação:
2 Al2O3(l)→4 Al3+(l) + 6 O2-(l)
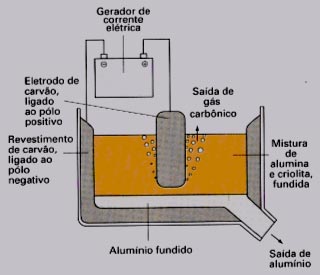
No recipiente, formado por ferro ou cobre, são acrescidos eletrodos de carbono para promover o processo de eletrólise. Apenas realizando essa etapa de eletrólise é possível produzir o metal de interesse. Como resultado, o próprio recipiente atua como cátodo, provocando a redução do íon alumínio. Com a finalidade de entender de forma mais clara essas etapas de oxidação e redução, estão representadas a seguir as semirreações do catodo e anodo e a de formação do gás carbônico, respectivamente:
4 Al3+(l) + 12 e–→ 4 Al(l) (semirreação do cátodo)
6 O2-(l) → 12 e– + 3º2(g) (semirreação do ânodo)
3 O2(g) + 3 C(s) → 3 CO2(g) (reação de formação do gás carbônico)
Desse modo, a reação global do processo Hall é:
2 Al2O3(l) + 3 C(s) → 4 Al(l) +3 CO2(g)
Principais usos do alumínio
Após analisar como ocorre o processo de produção do alumínio (Al(s)) é necessário compreender quais são as suas características, tanto físicas quanto químicas, que o torna muito importante na construção civil e no seguimento industrial, em geral. Entre as principais características, podemos destacar:
- Ponto de fusão de 660°C, sendo relativamente baixo se comparado ao aço;
- Peso específico de, aproximadamente, 2,70 g/cm³, muito menor que do cobre e aço por exemplo;
- Elevada resistência à corrosão por apresentar uma camada de óxido que o protege;
- Boa condutibilidade elétrica e térmica;
- não apresenta características magnéticas;
- Material facilmente reciclado, por não perder suas características após ser utilizado.
A partir disso, vamos destacar algumas aplicações importantes desse material.
Produção de foguetes e automóveis

As ligas de alumínio contém certas quantidades de cobre, manganês, silício e magnésio, entre outros materiais. Com isso, ela adquire elevada resistência mecânica, podendo ser largamente utilizada na indústria aeroespacial para fabricação de foguetes. Além disso, pode ser utilizada para fabricação de carrocerias de ônibus e caminhão, elementos estruturais de aviões, bicicletas, tanques.
Construção civil

Por apresentar durabilidade de aproximadamente 40 anos, resistência à corrosão e a facilidade de reciclagem, o alumínio pode ser utilizado na construção civil como estruturas provisórias (escoras e andaimes), fachadas em torno de vidros e na produção de janelas e portas.
Fabricação de latas

Por ser rapidamente fabricado, devido a propriedade de condutibilidade elétrica, o material é largamente utilizado como latas para cervejas, refrigerantes e tintas.
Utensílio de cozinha

O alumínio é largamente utilizado para produção de panelas e talheres devido, principalmente, à sua elevada condutividade térmica e resistência a corrosão.
Portanto, a partir da análise do processo de obtenção do alumínio, podemos compreender a importância do mineral criolita. Uma vez que, foi após o desenvolvimento do método Hall-Héroult, tendo a criolita como um dos agentes mais importantes, que o custo de produção do alumínio foi reduzido, passando a ser utilizado, a partir de então, em diversos produtos que utilizamos no dia a dia.
Autora: Nathália Bueno
Gostou do texto? Confira outros conteúdos em nosso blog e conheça nossos serviços! Entre em contato conosco por meio de nosso telefone (31) 3409-1033 / (31) 97167-5141, e-mail minasjr@minasjr.com.br ou redes sociais facebook e instagram, e veja o que podemos fazer por você!
